
 |
L´une des principales difficultés en hygrométrie est qu´il n´existe pas de relation exacte permettant de relier l´humidité relative et la température de rosée pour une température ambiante et une pression données. Ainsi, lorsque l´on veut connaître l´ensemble des paramètres de l´air humide à partir de l´humidité relative (par exemple avec un hygromètre à variation d´impédance), de la température de rosée (par exemple avec un hygromètre à condensation) ou de la température humide (avec un psychromètre) il est nécessaire de recourir à des modélisations. Le tableau 1 réalisé à partir de la référence [1] donne les grandeurs mesurées pour plusieurs types d´hygromètres.
| Type d´hygromètre | Principe physique de la mesure | Grandeur mesurée |
| « A condensation » | Mesure de la température de rosée ou de gelée. | Température de rosée ou de gelée. |
| « Capacitif » | Mesure de la capacité d´un diélectrique polymère. | Humidité relative. |
| « Résistif » | Mesure de la résistivité d´un corps hygroscopique. | Humidité relative. |
| « A oxyde métallique » | Mesure de la capacité d´un diélectrique. | Température de rosée ou de gelée. |
| « A sorption » | Mesure de la température d´équilibre d´une solution saline saturée. | Température de rosée ou de gelée. |
| « Electrolytique » | Electrolyse de l´eau absorbée par de l´anhydride phosphorique. | Fraction molaire. |
| « Mécanique » | Changement de dimension de fibres naturelles ou synthétiques. | Humidité relative. |
| « Psychromètre » | Mesure de la température humide. | Température humide. |
L´emploi de modélisations rend rapidement les calculs fastidieux. D´autre part, plusieurs modélisations existent pour une même grandeur et introduisent souvent des incertitudes non négligeables dans les conversions. Enfin, il faut garder à l´esprit que si un appareil est étalonné en humidité relative (resp. en température de rosée) et qu´il possède une fonction donnant automatiquement la température de rosée (resp. l´humidité relative), celle-ci n´est pas couverte par l´étalonnage et introduit de ce fait des erreurs non maîtrisées. Il est alors préférable de recourir à un logiciel externe que l´on aura validé par ailleurs pour faire la conversion.
Remarque 1 : il convient d'être prudent avec les systèmes de conversion automatiques présents sur les hygromètres. L'expérience
montre en effet que les modèles employés sont souvent très simplifiés (par rapport aux modèles présentés dans ce dossier) et de ce fait très
approximatifs. Par exemple, en l'absence de mesure de pression sur les hygromètres, la plupart du temps l'influence de celle-ci est
négligée dans les calculs.
Remarque 2 : il ne faut jamais oublier que le principe physique d'un hygromètre le limite
à ne mesurer qu'une grandeur. La connaissance de la grandeur à mesurer doit alors guider l'utilisateur dans le choix de l'hygromètre
(par exemple à l'aide du tableau 1).
1. Définitions de base et modélisations
Dans les lignes qui suivent les températures sont notées avec la lettre grecque thêta θ lorsquil sagit de températures exprimées en degrés Celsius et avec le symbole T quand elles sont exprimées en kelvins.
L´air sec est un mélange de gaz composé essentiellement de diazote, de dioxygène, d´argon et de dioxyde de carbone. On y trouve égalent d´autres gaz dans des quantités moindres (néon, hélium, méthane, krypton, dihydrogène, oxyde de diazote, monoxyde de carbone et xénon). La composition de l´air sec n´est pas définie de manière rigoureuse, celui-ci variant d´un endroit à l´autre. Néanmoins, dans les calculs on suppose cette composition constante en considérant un air sec de référence dont on trouvera une définition dans le tableau 2 extrait de la référence [2].
| Constituant | Masse molaire \( M_{\text{i}} \) (en \( 10^{-3}~\text{kg}/\text{mol} \)) |
Fraction molaire \( x_{\text{i}} \) |
Contribution \( x_{\text{i}} \cdot M_{\text{i}} \) (en \( 10^{-3}~\text{kg}/\text{mol} \)) |
| N2 | 28,013 4 | 0,780 848 | 21,874 207 |
| O2 | 31,998 8 | 0,209 390 | 6,700 229 |
| Ar | 39,948 | 0,009 332 | 0,372 795 |
| CO2 | 44,010 | 0,000 40 | 0,017 604 |
| Ne | 20,18 | 18,2 × 10−6 | 0,000 367 |
| He | 4,0 | 5,2 × 10−6 | 0,000 021 |
| CH4 | 16,0 | 1,5 × 10−6 | 0,000 024 |
| Kr | 83,8 | 1,1 × 10−6 | 0,000 092 |
| H2 | 2 | 0,5 × 10−6 | 0,000 001 |
| N2O | 44 | 0,3 × 10−6 | 0,000 013 |
| CO | 28 | 0,2 × 10−6 | 0,000 006 |
| Xe | 131 | 0,1 × 10−6 | 0,000 013 |
La composition de cet air sec de référence permet de définir une masse molaire moyenne pour l´air sec Ma en le considérant comme un gaz moyen. Ce qui donne dans une première approximation une valeur de Ma prise à 28,965 46 × 10−3 kg/mol (valeur recommandée dans la formule CIPM-2007 [2]).
Remarque : en faisant le calcul de Ma d'après le tableau 1 on trouve en réalité Ma =28,965 371 987 2 g/mol ce qui entraîne un biais par rapport à la valeur de 28,965 46 g/mol recommandée dans la formule CIPM-2007. Par exemple pour des conditions ambiantes l'erreur due à l'arrondi engendre un biais de quelques 10−6 sur la valeur de la masse volumique de l'air. Le logiciel AntiSecos prend en compte cette particularité en proposant soit de forcer la valeur de Ma à 28,965 46 g/mol pour respecter la compatibilité avec la formule CIPM-2007 ou d'effectuer le calcul à partir d'une la table modifiable donnant la composition de l'air sec de référence que l'on souhaite utiliser.
La référence [2] introduit une modélisation permettant de calculer la masse molaire de l´air sec de manière plus exacte par la relation :
Ma =[(28,965 46 + 12,011 × (xCO2 − 0,000 4)] × 10−3 kg/mol . |
(1) |
Cette formule traduit que les variations de la fraction molaire du dioxyde de carbone ont une influence significative sur la masse molaire de l´air humide et suppose que ces variations sont compensées exactement par les variations de la fraction molaire du dioxygène.
L´air humide est un mélange d´air sec et de vapeur d´eau (uniquement à l´état gazeux). Dans cet air humide, si na est la quantité de matière d´air sec et nv la quantité de matière de vapeur d´eau, alors la fraction molaire de la vapeur d´eau est définie par :
| \( \begin{eqnarray} x_\text{v} = \dfrac{n_\text{v}}{n_\text{a} + n_\text{v}}\end{eqnarray} \) , | (2) |
et la fraction molaire de l´air sec est définie par :
| \( \begin{eqnarray}x_\text{a} = \dfrac{n_\text{a}}{n_\text{a} + n_\text{v}}\end{eqnarray} \) . | (3) |
L´humidité relative, notée Uw et exprimée en %, est définie de manière exacte par le rapport de la fraction molaire de la vapeur d´eau dans l´air humide (xv) à la fraction molaire de la vapeur d´eau dans ce même air humide si il était saturé (xsv) à la même température et à la même pression, ce qui s´écrit :
| \( \begin{eqnarray}U_\text{w} = (100~\text{%}) \cdot \dfrac{x_\text{v}}{x_\text{sv}}\end{eqnarray} \) . | (4) |
1.4. Pression de vapeur saturante au dessus de l´eau en phase pure (ew)
La pression de vapeur saturante en phase pure est la pression de vapeur dans
un état d´équilibre avec une surface plane d´eau. Cette pression
est notée ew.
Remarque : on définit de même la pression de vapeur en équilibre avec une
surface plane de glace notée ei.
Modélisation
La pression de vapeur saturante au dessus de l´eau en phase pure
ew, exprimée en pascals, est calculée entre 223,15 K et 373,15 K
(-50 °C et 100 °C) par la relation suivante qui est issue
de la référence
[3] :
| \( \begin{eqnarray}\ln~\left[ \dfrac{ e_\text{w}(T) }{ 1~\text{Pa} } \right] = A \cdot T^2 + B \cdot T + C + \dfrac{D}{T} + E \cdot \ln~( \dfrac{ T }{ 1~\text{K} })\end{eqnarray} \) , | (5) |
avec T la température en kelvin et les coefficients suivants :
| A = | 1,673 952 × 10−5 K−2 ; | |
| B = | −2,711 193 × 10−2 K−1 ; | |
| C = | 21,240 964 2 ; | |
| D = | −6 096,938 5 K ; | |
| E = | 2,433 502 . |
Validité du modèle
Dans la pratique cette modélisation est extrapolée en dehors de son domaine de définition. Le modèle employé est testé par comparaison
avec des valeurs de référence prises dans la référence
[4].
Les résultats sont présentés au paragraphe 3.1.1 dans le tableau 4 entre
-70 °C et 100 °C. Il n´y a pas d´écart constaté.
Remarque :
si on souhaite travailler avec des températures en degrés Celsius il faut faire le changement variable suivant :
T =θ + 273,15, ce qui donne léquation :
ln ew(θ + 273,15) =A·(θ + 273,15)2 + B · (θ + 273,15) + C + D/(θ + 273,15) + E·ln(θ + 273,15).
Dans la suite de larticle, par abus de langage on écrira ew(θ) pour désigner la pression
de vapeur saturante correspondant à une température en degrés Celsius. De même pour \( e_{\text{w}}(\theta) \), etc.
1.5. Facteur d´augmentation (f)
La pression de vapeur saturante de l´air humide par rapport à l´eau (\( e_\text{w}' \)) peut se déduire de \( e_\text{w} \) par la relation suivante :
| \( e_\text{w}' = f \cdot e_\text{w} \) , | (6) |
dans laquelle f est appelé le facteur d´augmentation. Ce facteur
proche de l´unité est quelquefois négligé en première
approximation. Il traduit le fait que l´air humide ne se comporte pas tout à
fait comme un gaz parfait.
Modélisation
Le facteur d´augmentation f est calculé entre 173,15 K
et 373,15 K (i.e. -100 °C et 100 °C)
par la relation suivante qui est extraite de la référence
[5] :
| \( \begin{eqnarray}f = \exp \left[\alpha \cdot \left(1 - \dfrac {e_\text{w}}{P}\right) + \beta \cdot \left(\dfrac {P}{e_\text{w}} - 1\right)\right]\end{eqnarray} \) , | (7) |
dans laquelle P est la pression absolue en pascals, ew, la pression de vapeur saturante en phase pure au dessus de l´eau et avec :
| \( \begin{eqnarray}\alpha = \sum_{i=0}^3 A_\text{i} \cdot T^\text{i}\end{eqnarray} \) et \( \begin{eqnarray}\ln~\beta = \sum_{i=0}^3 B_\text{i} \cdot T^\text{i}\end{eqnarray} \) , |
ou T est la température en kelvin.
Les valeurs des coefficients A0,
..., A3 et
B0, ...,
B3 sont données dans le tableau 3 par plage de température.
| Coefficients | Plages de température | |
| \( \left[173,15~\text{K}~;~273,15~\text{K}\right] \) | \( \left[273,15~\text{K}~;~373,15~\text{K}\right] \) | |
| i.e. \( \left[-100~\text{°C}~;~0~\text{°C}\right] \) | i.e. \( \left[0~\text{°C}~;~+100~\text{°C}\right] \) | |
| A0 | −5,589 810 1 × 10−2 | −1,630 204 1 × 10−1 |
| A1 | 6,714 038 9 × 10−4 K−1 | 1,807 157 0 × 10−3 K−1 |
| A2 | −2,749 272 1 × 10−6 K−2 | −6,770 306 4 × 10−6 K−2 |
| A3 | 3,826 895 8 × 10−9 K−3 | 8,581 360 9 × 10−9 K−3 |
| B0 | −8,198 539 3 × 101 | −5,989 046 7 × 101 |
| B1 | 5,823 082 3 × 10−1 K−1 | 3,437 804 3 × 10−1 K−1 |
| B2 | −1,634 052 7 × 10−3 K−2 | −7,732 639 6 × 10−4 K−2 |
| B3 | 1,672 508 4 × 10−6 K−3 | 6,340 528 6 × 10−7 K−3 |
Validité du modèle
Le modèle employé est testé par comparaison avec des valeurs de référence prises dans la référence
[8].
Les résultats sont présentés au paragraphe 3.1.2 dans le tableau 7. Le modèle est aussi testé par rapport aux valeurs de la référence
[3]
qui couvre des gammes plus importantes de pression et de température. Les résultats sont présentés au paragraphe 3.1.2 dans le tableau 8. Dans
tous les cas, les écarts sont au plus égal à la résolution.
Remarque :
d'après l'équation (7), le facteur d'augmentation f dépend de
la pression P et de la température T. En toute rigueur
on doit donc l'écrire f(P, T). Si on souhaite utiliser des températures en degrés
Celsius, il faudrait en toute rigueur écrire f(P, θ + 273,15). Dans la
suite de cet article, par abus de langage, on écrira f(P, θ) pour désigner
le facteur d'augmentation à la pression P et à la température θ.
1.6. Pression partielle de la vapeur d´eau (e')
Pression qu´exercerait la vapeur d´eau si elle occupait seule le volume considéré.
1.7. Température de rosée (θd)
La température de rosée, notée θd est la température à laquelle il faut refroidir l´échantillon d´air humide pour provoquer la saturation, le rapport de mélange (cf. §1.11) restant constant. Par définition, la pression partielle de la vapeur d´eau vaut alors :
| \( e' = e_w' (\theta_\text{d}) \). | (8) |
1.8. Détermination de l´humidité relative à partir de la température de rosée
En appliquant à l´air humide que l´on considère comme un gaz parfait la loi de Dalton, et compte tenu de la définition du point de rosée, il vient :
| \( \begin{eqnarray}U_\text{w} = \left( 100~\text{%} \right) \times \dfrac{ e_\text{w}'~(T_\text{d}) }{ e_\text{w}'~(T_\text{s}) } = \left( 100~\text{%} \right) \times \dfrac{ f(P,~T_\text{d}) }{ f(P,~T_\text{s}) } \times \dfrac{ e_\text{w}~(T_\text{d}) }{ e_\text{w}~(T_\text{s}) }\end{eqnarray} \) , | (9) |
avec :
|
Td : la température de rosée ;
|
Remarque : cette relation permet de calculer de manière approchée la température de rosée à partir de l´humidité relative pour une pression et une température sèche données.
1.9. Calcul de la fraction molaire de la vapeur d'eau (xv)
La fraction molaire de la vapeur d'eau est définie d'après la relation (2) :
| \( \begin{eqnarray}x_\text{v} = \dfrac{n_\text{v}}{n_\text{a} + n_\text{v}}\end{eqnarray} \) . | |
En utilisant la pression de l'air humide (p), d'après la loi de Dalton et la relation (8), on a :
| \( \begin{eqnarray}x_\text{v} = \dfrac{e_\text{w}' (\theta_\text{d})}{ p }\end{eqnarray} \) . | |
D'après la relation (6) on déduit l'expression de la fraction molaire de la vapeur d'eau à partir de la pression et de la température de rosée :
| \( \begin{eqnarray}x_\text{v} = \dfrac{f(P,~\theta_\text{d}) \cdot e_\text{w} (\theta_\text{d})}{p}\end{eqnarray} \) . | (10) |
Si on ne dispose que de l'humidité relative, en utilisant la formule (9), on transforme la formule (10) :
| \( \begin{eqnarray}x_\text{v} = \dfrac {U_\text{w}}{ 100~\text{%} } \cdot \dfrac{f(P,~\theta_\text{s}) \cdot e_\text{w} (\theta_\text{s})}{p}\end{eqnarray} \) . | (11) |
1.10. Facteur de compressibilité (Z)
Le facteur de compressibilité Z traduit le fait que l´air humide ne se comporte pas tout à fait comme un gaz parfait (interaction entre les molécules de l´air sec et de l´eau, etc.). Celui-ci permet d´appliquer la loi des gaz parfaits à l´air humide en écrivant :
| \( p \cdot V = n \cdot Z \cdot R \cdot T \) . | (12) |
La référence [6] donne une formule approchée permettant de calculer Z pour des pressions entre 60 000 Pa et 110 000 Pa, et, des températures entre 15 °C et 27 °C :
| \( \begin{eqnarray}Z = 1 - \dfrac{p}{T} \cdot \left[ a_0 + a_1 \cdot \theta + a_2 \cdot \theta^2 + (b_0 + b_1 \cdot \theta) \cdot x_\text{v} + (c_0 + c_1 \cdot \theta) \cdot x_\text{v}^2\right] + \dfrac{p^2}{T^2} \cdot (d + e \cdot x_\text{v}^2)\end{eqnarray} \) , | (13) |
avec :
| T | : la température en kelvin ; | |
| θ | : la température en degrés Celsius (θ =T − 273,15) ; | |
| p | : la pression absolue en pascals ; | |
| xv | : la fraction molaire de la vapeur d´eau ; |
et les coefficients suivants :
| a0 | = | 1,581 23 × 10−6 K · Pa−1 ; | |
| a1 | = | 2,933 1 × 10−8 Pa−1 ; | |
| a2 | = | 1,104 3 × 10−10 K−1 · Pa−1 ; | |
| b0 | = | 5,707 × 10−6 K · Pa−1 | |
| b1 | = | 5,707 × 10−6 K · Pa−1 | |
| c0 | = | 1,989 8 × 10−4 K · Pa−1 ; | |
| c1 | = | −2,376 × 10−6 Pa−1 ; | |
| d | = | 1,83 × 10−11 K2 · Pa−2 ; | |
| e | = | −0,765 × 10−8 K2 · Pa−2 . |
Le rapport de mélange est le rapport de la masse de vapeur d´eau (mv) à la masse d´air sec (ma) :
| \( \begin{eqnarray}r = \dfrac{m_\text{v}}{m_\text{a}}\end{eqnarray} \) . | (14) |
L'unité de cette grandeur est kg/kg et s'exprime généralement sans unité. Toutefois, ses valeurs étant généralement très faibles, il est d'usage de les manipuler en les multipliant par 1 000, ce qui revient à l'exprimer en grammes de vapeur d'eau par kilogramme d'air sec g/kg. On peut également multiplier les valeurs par 106, ce qui revient à l'exprimer en ppm (partie par million), quelques fois noté ppmm pour insister sur le fait qu'il s'agit de parties par million en masse.
Le rapport de mélange est une notion relevant du domaine de la chimie. Il existe deux types de rapport de mélange : massique et molaire [7]. Dans le domaine de l'hygrométrie, on parle de « rapport de mélange ». Cette expression, souvent utilisée en météorologie, est incomplète et devrait être « rapport de mélange massique ». Cette appellation est d'autant plus rendue nécessaire qu'il existe un autre rapport de mélange utilisé en hygrométrie. Pour cette raison afin d'éviter toute confusion, on utilisera par la suite le symbole rmas pour désigner cette grandeur.
La loi de Dalton et la loi des gaz parfaits à l'équation (14) conduisent à la relation :
| \( \begin{eqnarray}r_{\text{mas}} = \dfrac{ M_\text{v} }{ M_\text{a} } \cdot \dfrac{ e' }{p - e'}\end{eqnarray} \) . | (15) |
avec :
| Mv | : la masse molaire de l'eau ; | |
| Ma | : la masse molaire de l'air sec ; | |
| e' | : la pression partielle de la vapeur d'eau ; | |
| p | : la pression absolue. |
1.12. Rapport de mélange molaire (rmol)
Le rapport de mélange molaire, que l'on notera rmol, est le rapport entre le nombre de moles de vapeur d'eau nv et le nombre de moles d'air sec na :
| \( \begin{eqnarray}r_{\text{mol}} = \dfrac{n_\text{v}}{n_\text{a}}\end{eqnarray} \) . | (16) |
L'unité de cette grandeur est donc mol/mol et s'exprime généralement sans unité. Toutefois, ses valeurs étant généralement très faibles, il est d'usage de les manipuler en les multipliant par 106, ce qui revient à les exprimer en ppm (partie par million). Compte tenu qu'il existe également un rapport de mélange massique, l'emploi des ppm introduit un risque de confusion. Il semble plus judicieux dans ce cas d'exprimer le résultat en µmol/mol, ce qui en plus présente l'avantage de respecter les conventions d'écriture du Système International dunités.
Autres expressions du rapport de mélange molaire :
De façon triviale, on a :
| \( \begin{eqnarray}r_{\text{mol}} = \dfrac{x_\text{v}}{x_\text{a}}\end{eqnarray} \) , | (17) |
avec xv et xa les fractions molaires de la vapeur d'eau et de l'air sec.
Dautre part, en appliquant la loi des gaz parfaits on a :
| \( \begin{eqnarray}n_{\text{v}} = \dfrac{ e'_\text{v} \cdot V }{ R \cdot T }\end{eqnarray} \) , | (18) |
et :
| \( \begin{eqnarray}n_{\text{a}} = \dfrac{ p_\text{a} \cdot V }{ R \cdot T }\end{eqnarray} \) , | (19) |
avec :
| e' | : la pression partielle de la vapeur d'eau ; | |
| pa | : la pression partielle de l'air sec ; | |
| R | : la constante molaire des gaz ; | |
| V | : le volume occupé par l'air humide. |
D'où :
| \( \begin{eqnarray}r_{\text{mol}} = \dfrac{ e' }{ p - e' }\end{eqnarray} \) , | (20) |
en notant p la pression de l'air humide (p =pa + e').
Remarque : dans les domaines de la météorologie, des études sur le climat et chez les constructeurs d'hygromètres on rencontre souvent l'expression « rapport de mélange volumique » (mixing volume ratio en langue anglaise) dont l'unité est exprimée ppmv (parties par million en volume). Cette expression est surprenante car elle ne correspond à aucun des rapports de mélange définis par les chimistes [7]. Elle est généralement définie comme le quotient entre les pressions partielles de vapeur d'eau et d'air sec, ce qui correspond à l'équation (20). En d'autres termes, l'expression « rapport de mélange volumique » est fausse et ne doit pas être utilisée : il s'agit en réalité d'un rapport de mélange molaire.
1.13. Enthalpie spécifique de l´air humide (h)
L´enthalpie de l´air humide est définie comme la quantité de chaleur totale à fournir à 1 kg d´air sec initialement à la température de 0 °C pour le porter à la température θ et à un rapport de mélange r.
Remarque 1 : ainsi définie, l´enthalpie spécifique est la chaleur totale contenue dans l´air humide en prenant pour origine des enthalpies l´air sec à 0 °C.
Remarque 2 : si h1 est l´enthalpie d´un échantillon d´air humide dans l´état E1(θ1, r1) et h2 dans l´état E2(θ2, r2) alors l´énergie à fournir pour passer l´échantillon d´air contenant la masse ma d´air sec de l´état E1 à l´état E2 est : (h2 − h1) · ma.
Modélisation
L´enthalpie de l´air humide est calculée par la relation
exacte :
| \( h = Cp_\text{a} \cdot \theta + r \cdot (L_0 + Cp_\text{v} \cdot \theta) \) , | (21) |
dans laquelle Cpa est la chaleur massique de l´air sec, θ la température de l´air humide en degrés Celsius, r le rapport de mélange, L0 la chaleur latente de vaporisation de l´eau à 0 °C et Cpv la chaleur massique de la vapeur d´eau à 0 °C et 101 325 Pa. Cpa, Cpv et L0 sont calculées avec les modélisations suivantes :
|
\( Cp_\text{a} = 1,005~67 + 1,603~5 \times 10^{-5} \times \theta \) ;
|
avec θ la température sèche en °C.
L´humidité spécifique est le rapport entre la masse d´eau mv et la masse d´air humide (ma + mv) dans laquelle se trouve la masse de vapeur d´eau :
| \( \begin{eqnarray}q = \dfrac{m_\text{v}}{m_\text{a} + m_\text{v}}\end{eqnarray} \) . | (22) |
Dans la pratique, l´humidité spécifique peut être calculé à partir du rapport de mélange r par la formule :
| \( \begin{eqnarray}q = \dfrac{r}{1 + r}\end{eqnarray} \) . | (23) |
Remarque : dans cette formule, r doit être exprimé en « kg/kg ».
1.15. Masse volumique de l´air humide (ρah)
La masse volumique de l'air est déterminée par une formule communément appelée « formule du CIPM ». Cette formule utilise des paramètres de l'air humide plus facilement accessibles — que la masse volumique elle-même — au moyen de l'instrumentation disponible. Elle repose sur la loi des gaz parfaits. Elle est rendue compatible avec l'air humide au moyen du facteur de compressibilité de ce gaz. En introduisant la pression de vapeur saturante de l'air humide par rapport à l'eau (elle-même calculée à partir de la pression de vapeur saturante au-dessus de l'eau en phase pure et du facteur d'augmentation de l'air humide), la masse volumique de l'air est alors calculée à partir de la température sèche, la pression de l'air et l'humidité relative ou la température de rosée. Afin d'améliorer l'exactitude de cette formule, celle-ci a été aménagée pour prendre en compte les variations de la fraction molaire du dioxyde de carbone dans l'air.
Cette formule a été recommandée par la 17e
CGPM de 1893 (3e résolution)
[8]
et révisée par le CIPM en 1991
[6]
puis en 2007
[2].
A l'issue de chacune de ces trois étapes, la formule a été notée successivement :
– CIPM-81 ;
– CIPM-81/91 ;
– CIPM-2007.
Depuis sa version initiale (CIPM-81), la formule n'a pas été modifiée.
Les modifications ont concerné les valeurs de coefficients et de constantes. La révision de la
formule en 1991 (CIPM-81/91) a porté sur le changement des valeurs de coefficients dans les
modélisations :
– du facteur d'augmentation de l'air humide ;
– de la pression de vapeur saturante de l'eau en phase pure ;
– du facteur de compressibilité de l'air humide.
Il n y a pas eu de nouvelles données pour le calcul de ces modélisations. Les modifications sont la conséquence du changement d'échelle de température de 1990 lié au passage de l'EIPT-68 à l'EIT-90 [10]. D'autre part, la constante molaire des gaz a été mise à jour pour prendre en compte la valeur du Codata de 1986. La révision de la formule de 2007 (CIPM-2007) porte sur la modification de la fraction molaire des constituants de l'air sec de référence (tableau 4).
| Constituant | Masse molaire \( M_\text{i} \) (en \( 10^{-3}~\text{kg/mol} \)) |
Fraction molaire \( x_\text{i} \) |
Contribution \( x_\text{i} \cdot M_\text{i} \) (en \( 10^{-3}~\text{kg/mol} \)) |
| N2 | 28,013 4 | 0,781 01 | 21,878 746 |
| 0,780 848 | 21,874 207 | ||
| O2 | 31,998 8 | 0,209 39 | 6,700 229 |
| 0,209 390 | 6,700 229 | ||
| Ar | 39,948 | 0,009 17 | 0,366 323 |
| 0,009 332 | 0,372 795 | ||
| CO2 | 44,010 | 0,000 40 | 0,017 604 |
| 0,000 40 | 0,017 604 | ||
| Ne | 20,18 | 18,2 × 10−6 | 0,000 367 |
| 18,2 × 10−6 | 0,000 367 | ||
| He | 4,0 | 5,2 × 10−6 | 0,000 021 |
| 5,2 × 10−6 | 0,000 021 | ||
| CH4 | 16,0 | 1,5 × 10−6 | 0,000 024 |
| 1,5 × 10−6 | 0,000 024 | ||
| Kr | 83,8 | 1,1 × 10−6 | 0,000 092 |
| 1,1 × 10−6 | 0,000 092 | ||
| H2 | 2 | 0,5 × 10−6 | 0,000 001 |
| 0,5 × 10−6 | 0,000 001 | ||
| N2O | 44 | 0,3 × 10−6 | 0,000 013 |
| 0,3 × 10−6 | 0,000 013 | ||
| CO | 28 | 0,2 × 10−6 | 0,000 006 |
| 0,2 × 10−6 | 0,000 006 | ||
| Xe | 131 | 0,1 × 10−6 | 0,000 013 |
| 0,1 × 10−6 | 0,000 013 |
La principale modification est liée à une nouvelle détermination de la fraction molaire de l'argon. La variation de la fraction molaire du diazote est la conséquence de la nouvelle fraction molaire de l'argon. D'autre part, la constante molaire des gaz a été mise à jour pour prendre en compte la valeur du Codata de 2006. Les différentes modifications opérées sur la formule du CIPM sont résumées dans le tableau 5.
| CIPM-81 | CIPM-81/91 | CIPM-2007 | |
| Formule | La formule est construite à partir de la loi des gaz parfaits. | / | / |
| Composition de l'air sec | Mesures effectuées essentiellement au début du XXe siècle. | / | Nouvelle fraction molaire de l'argon. |
| Constante molaire des gaz | Valeur du Codata de 1972 | Valeur du Codata de 1986 | Valeur du Codata de 2006 |
| Facteur d'augmentation de l'air humide (modélisation) | Modélisation (selon l'EIPT-68) à partir de données de Wexler et Greenspan de 1976 | Modification pour rendre la modélisation compatible avec l'EIT-90. | / |
| Pression de vapeur saturante de l'eau en phase pure (modélisation) | Modélisation (selon l'EIPT-68) à partir de données de Wexler et Greenspan de 1976 | Modification pour rendre la modélisation compatible avec l'EIT-90. | / |
| Facteur de compressibilité de l'air humide (modélisation) | Modélisation (selon l'EIPT-68) à partir de données de Hyland de 1975 | Modification pour rendre la modélisation compatible avec l'EIT-90. | / |
La formule extraite de la référence [8] à la forme suivante :
| \( \begin{eqnarray}\rho_\text{ah} = \dfrac{ p \cdot M_\text{a} }{ Z \cdot R \cdot T } \cdot \left[1 - x_\text{v} \cdot \left(1 - \dfrac{ M_\text{v} }{ M_\text{a} }\right)\right]\end{eqnarray} \) , | (24) |
avec :
| p | : la pression absolue en pascals (à mesurer avec un baromètre) ; | |
| T | : la température en kelvin (à mesurer avec un thermomètre) ; | |
| xv | : la fraction molaire de la vapeur d'eau (à calculer par la relation (10) ou (11)) ; | |
| Ma | : la masse molaire de l'air sec (à calculer par la relation (1)) ; | |
| R | : la constante molaire des gaz (R =8,314 472 J/mol [11]) ; | |
| Mv | : la masse molaire de l'eau (Mv =18,015 28 × 10−3 kg/mol [12]) ; | |
| Z | : le facteur de compressibilité (à calculer par la relation (13)). |
Le volume spécifique, noté Vs, est le
volume occupé par l´air humide contenant 1 kg d´air sec.
Le volume spécifique est calculé en utilisant la relation (exacte) suivante :
| \( \begin{eqnarray}V_\text{s} = \dfrac{ R \cdot T }{ M_\text{v} \cdot \rho } \cdot (\delta + r)\end{eqnarray} \) , | (25) |
avec :
|
R : la constante molaire des gaz ;
|
Pour les calculs, les valeurs suivantes sont conseillées :
|
R = 8,314 472 J/mol
[11] ;
|
L´humidité absolue est le rapport entre la masse de vapeur d´eau mv et le volume V occupé par l´air humide considéré dans les conditions de pression et de température données, ce qui s´écrit :
| \( \begin{eqnarray}\rho_\text{v} = \dfrac{m_\text{v}}{V}\end{eqnarray} \) . | (26) |
La température humide est la température d'équilibre
d'une masse d'eau s'évaporant dans l'air humide dans le cas ou la
chaleur nécessaire à l'évaporation n'est
prélevée que dans l'air humide. La température humide est
utilisée le plus souvent lors de l'emploi d'un psychromètre. Le
psychromètre est un hygromètre composé de deux thermomètres
ventilés avec l'air humide étudié. L'un des deux
thermomètres est recouvert d'une gaze humidifiée.
L'évaporation de l'eau s'effectue en prélevant de la chaleur,
ce qui provoque un abaissement de la température mesurée par le
thermomètre recouvert par la gaze humide. A l'équilibre, la
température mesurée par ce thermomètre est la température
humide.
On démontre que moyennant quelques simplifications, la relation entre la
température humide et la température de rosée peut se mettre sous
la forme :
| \( e_\text{w}'~(T_\text{d},~p) = e_\text{w}'~(T_\text{w},~p) - A \cdot p \cdot (T - T_\text{w}) \) , | (27) |
avec :
| Td : la température de rosée ; | |
| Tw : la température humide ; | |
| p : la pression de l'air humide ; | |
| A : le coefficient psychrométrique ; | |
| \( e_\text{w}'~(T_\text{d},~p) \) : la pression partielle de vapeur d'eau ; | |
| \(e_\text{w}'~(T_\text{w},~p) \) : la pression de vapeur saturante à la température humide. |
Remarque : la relation (8) est quelquefois appelée
« équation psychrométrique ».
En écrivant le phénomène physique qui conduit à
l'équation (8) on trouve en réalité que A
vaut après simplification :
| \( \begin{eqnarray}A = \dfrac{ M_\text{a} \cdot C_\text{pa} }{ M_\text{v} \cdot L_\text{w} }\end{eqnarray} \) , | (28) |
avec :
|
Cpa : la chaleur massique à pression constante de l'air sec ;
|
Remarque : quelquefois, A est appelé
« constante psychrométrique », ce qui est
erroné puisque ce n'est pas une constante en toute rigueur.
L'équation (9) permet d'affecter à A une valeur dans une
première approximation. Néanmoins, lors de l'utilisation d'un
psychromètre réel, le fonctionnement ne respecte pas toujours rigoureusement
le processus physique décrit par les équations (8) et (9) : apports de
chaleur extérieur (rayonnement, conduction), modification de la température
localement au voisinage du thermomètre humide, etc. Ainsi, il est souvent
commode d'affecter à A une valeur déterminée lors de
l'étalonnage du psychromètre.
Remarque : d'après la référence
[3],
il est courant d'obtenir pour des psychromètres ventilés des valeurs comprises entre
A =6,4 × 10−4 °C−1 et
A =6,8 × 10−4 °C−1.
Le logiciel AntiSecos met en oeuvre l´ensemble des formules énumérées dans le premier chapitre. Trois cas de figure se présentent habituellement : 1) on dispose de l´humidité relative ; 2) on dispose de la température de rosée ; 3) on dispose de la température humide.
D´après le tableau 1, ce cas de figure peut correspondre à : un hygromètre capacitif, un hygromètre résistif ou un hygromètre mécanique. Sur le logiciel AntiSecos, il faut alors sélectionner « hygromètre à variation d´impédance ». L´écran de la figure 1 apparaît alors.
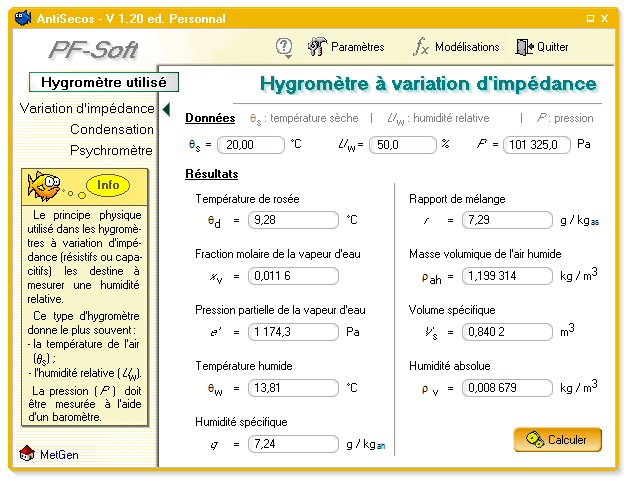
D´après le tableau 1, ce cas de figure peut correspondre à : un hygromètre à condensation, un hygromètre oxyde métallique ou un hygromètre à sorption. Sur le logiciel AntiSecos, il faut alors sélectionner « hygromètre à condensation ». L´écran de la figure 2 apparaît alors.

D´après le tableau 1, ce cas de figure correspond à un psychromètre. Sur le logiciel AntiSecos, il faut alors sélectionner « Psychromètre ». L´écran de la figure 3 apparaît alors.

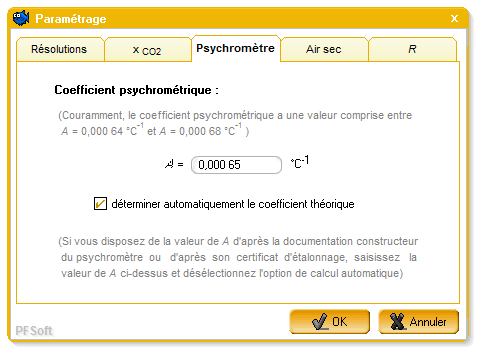
Pour l'ensemble des calculs de température humide,
AntiSecos offre la possibilité de saisir un coefficient
psychrométrique spécifique à l'appareil (provenant d'un
étalonnage ou de la documentation constructeur) ou d'évaluer un
coefficient théorique comme le montre la figure 4.
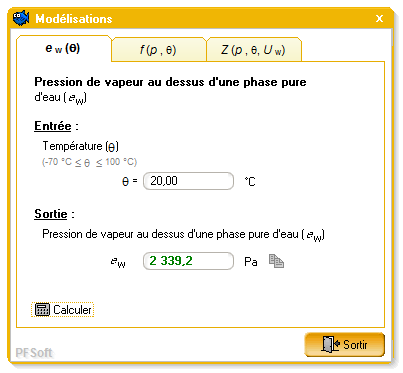
Les formulaires de calcul des fonctions de base sont accessibles en cliquant sur le bouton « Modélisations ».
2.4.1. Pression de vapeur au dessus d´une phase pure d´eau
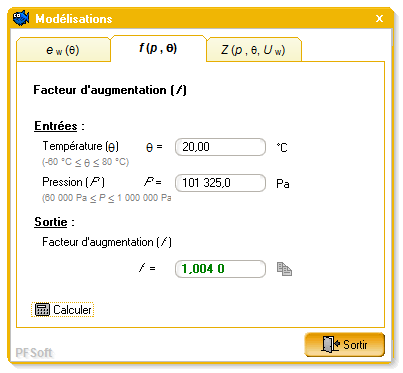
2.4.3. Facteur de compressibilité
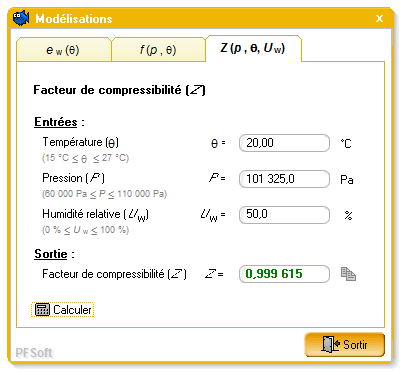
2.5.1. Composition de l´air sec
Comme indiqué au 1.1, l'air sec est défini comme un gaz moyen comprenant différents constituants dans certaines proportions. A partir des masses molaires de ces différents constituants et de leurs proportions on calcule une masse molaire moyenne, notée Ma, correspondant à cet air sec. La valeur de Ma a une incidence sur les grandeurs suivantes :
Les travaux les plus avancés pour le calcul de Ma sont ceux effectués dans le cadre de la formule du CIPM-2007 [2]. Le logiciel AntiSecos permet de modifier le calcul de Ma au travers de l'écran de paramétrage représenté sur la figure 8.
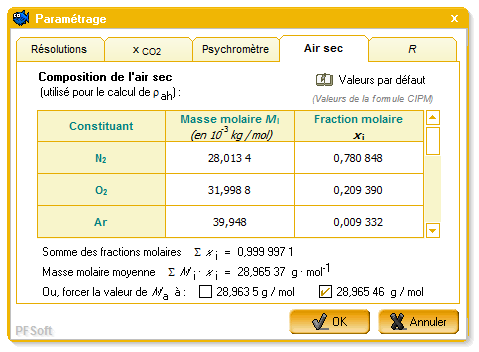
Les différents constituants de l'air sec, leur masse molaire et leur fraction molaire sont enregistrés pour le calcul de Ma. En cliquant sur « valeurs par défaut », le logiciel propose de charger les valeurs de la formule CIPM-2007 [2] ou à des fins historiques les valeurs de la formule CIPM-81/91 ([6], [8]). Il est également possible de modifier les valeurs des masses molaires ou des fractions molaires en double cliquant sur les cellules du tableau. Toutefois comme le précise le paragraphe 1.1, les valeurs de Ma calculées à partir des constituants ou figurant dans les formules du CIPM sont légèrement différentes, en raison d'arrondis. Afin d'assurer une compatibilité avec les formules du CIPM, le logiciel AntiSecos propose de forcer les valeurs de Ma à :
Lorsque la valeur de Ma est forcée à l'une de ces deux valeurs, le terme correctif lié à la fraction molaire de CO2, défini au travers de l'écran de la figure 9, est pris en compte selon la formule (1).
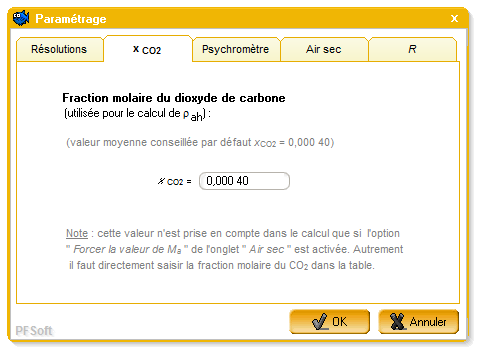
2.5.2. Constante molaire des gaz
La constante molaire des gaz impacte directement les grandeurs suivantes :
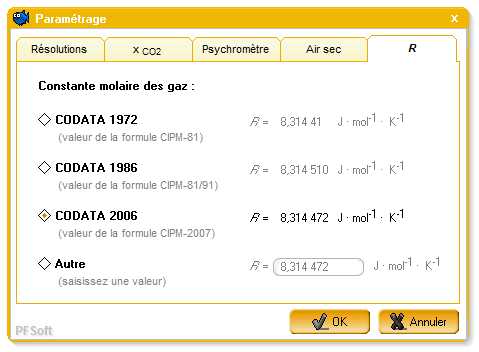
Cette constante est déterminée régulièrement par différentes équipes de recherche et les valeurs retenues sont publiées dans le cadre du Codata. Le logiciel AntiSecos permet de choisir les valeurs de la constante molaire des gaz qui ont été utilisées dans le cadre des formules du CIPM ou de définir toute autre valeur comme indiqué sur la figure 10.
La principale cause d´erreur sur les calculs effectués provient des modèles employés. Ainsi, les essais réalisés portent avant tout sur les modèles ou fonctions de base : pression de vapeur saturante en phase pure au dessus d´une surface d´eau, facteur d´augmentation, facteur de compressibilité. Ils ont consisté à comparer les valeurs obtenues avec AntiSecos aux valeurs données par un certain nombre de publications internationales. D´autre part, la première étape dans les calculs (pour déduire ensuite l´ensemble des paramètres de l´air humide) consistant à convertir l´humidité relative en température de rosée (et réciproquement), cette étape a fait l´objet d´une validation spécifique (cf. § 3.2.1.).
3.1.1. Pression de vapeur saturante en phase pure au dessus de l´eau (ew)
Une série de 171 valeurs de pression de vapeur saturante en phase pure au dessus de l´eau pour des températures comprises entre −70 °C et 100 °C variant avec un pas de 1 °C ont été comparées entre :
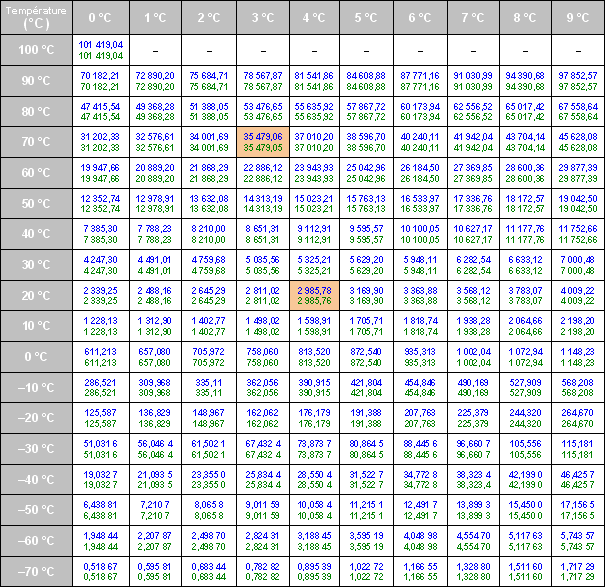
3.1.2. Facteur d´augmentation (f )
Une série de 77 valeurs du facteur d´augmentation pour des températures comprises entre 0 °C et 30 °C variant avec un pas de 5 °C et des pressions variant entre 60 000 Pa et 110 000 Pa avec un pas de 5 000 Pa ont été comparées entre :
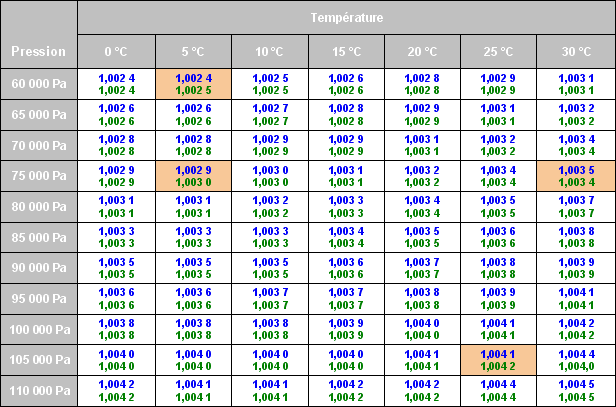
Une série supplémentaire de 32 valeurs a été testée pour couvrir des valeurs extrêmes de températures (entre -60 °C et 80 °C) et de pressions (entre 101 300 Pa et 1 000 000 Pa). Les valeurs obtenues par AntiSecos (en vert dans le tableau 8) ont été comparées aux valeurs de la référence [3] (en bleu dans le tableau 8).
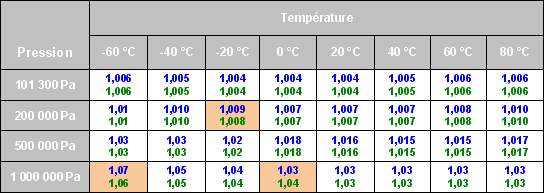
Une série de 119 valeurs de l´humidité relative pour des températures sèches comprises entre 0 °C et 100 °C et des températures de rosée comprises entre 0 °C et 90 °C pour ont été comparées entre :
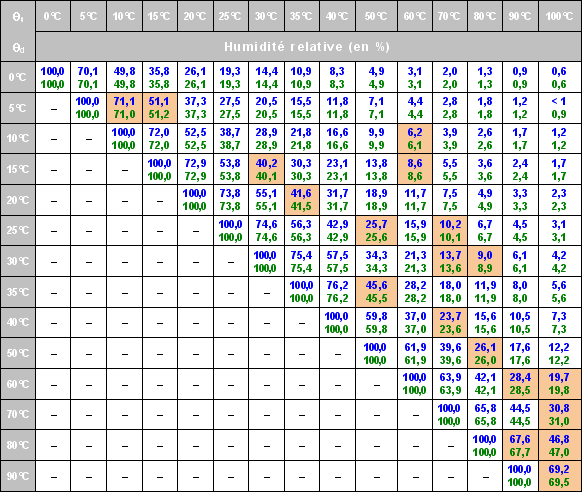
Jusqu´à 60 °C, les écarts en humidité relative sont inférieurs à 0,1 % et à 0,3 % jusqu´à 90 °C. Ces écarts sont très faibles devant les incertitudes rencontrées en hygrométrie comme le montre le tableau 10 réalisé à partir de la référence [1].
| Type d´hygromètre | Grandeurs mesurées | Incertitude de mesure (sur la grandeur mesurée) |
| « A condensation | Température de rosée ou de gelée | 0,2 °C à 0,5 °C |
| « Capacitif » | Humidité relative | 2 % à 5 % |
| « Résistif » | Humidité relative | 2 % à 5 % |
| « A oxyde métallique » | Température de rosée ou de gelée | 2 °C à 3 °C |
| « A sorption » | Température de rosée ou de gelée | 1 °C à 3 °C |
| « Electrolytique » | Fraction molaire | 5 % de l´échelle |
| « Mécanique » | Humidité relative | 10 % |
| « Psychromètre » | Température humide | 0,2 °C à 1 °C |
3.2.2. Masse volumique de l´air (ρah)
Une série 4 valeurs de la masse volumique de l´air humide ont été comparées pour différentes valeurs de la pression, l´humidité relative et la température sèche entre :
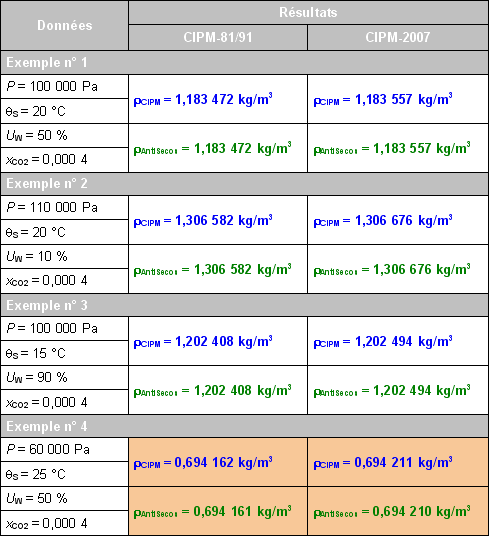
Remarque : on se reportera aux paragraphes 2.5.1 et 2.5.2 pour la définition des paramétrages liés aux formules CIPM-81/91 et CIPM-2007.
Concernant la formule CIPM-81/91, les données de référence sont extraites de [6]. S'agissant de la formule CIPM-2007, au moment de la rédaction de ce dossier il n'existait pas de jeux de données de référence permettant de tester les calculs. Ce point est manquant et aurait dû être inclus dans les publications présentant la formule CIPM-2007, comme cela avait été fait pour les formules précédentes. Un jeu de données a donc été calculé directement avec le logiciel PFS-AC [13]. L'équation correspondante peut être téléchargée dans le lien suivant (décompresser l'archive zip dans le répertoire de l'application PFS-AC) :
 |
équation PFS-AC permettant de générer les valeurs de référence. |
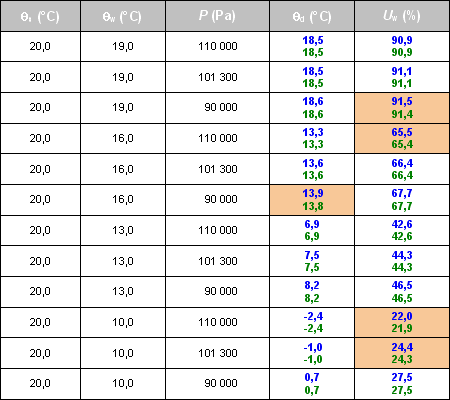
3.2.3. Température humide (θw)
Une série 12 valeurs de l'humidité relative Uw (et de la température de rosée θd) calculées à partir de la température sèche θs, la température humide θw et la pression P ont été comparées entre :
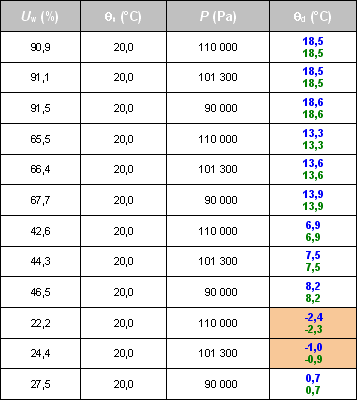
Vérification de la fonction réciproque
| [1] | « Mesure de l´humidité de l´air - Généralités sur les instruments de mesure », Afnor, 1993. |
| [2] | PICARD A., DAVIS R.S. et FUJII K., "Revised formula for the density of moist air (CIPM-2007)", Metrologia, 45, 2008, 149-155. |
| [3] | "A guide to the measurement of humidity", National Physical Laboratory, Teddington. |
| [4] | « Mesure de l´humidité de l´air - Paramètres hygrométriques », Afnor, 1994. |
| [5] | HARDY B., "ITS-90 Formulations for vapor pressure, frostpoint temperature, dewpoint temperature, and enhancement factors in the range -100 to +100 °C", Proceedings of the Third International Symposium on Humidity & Moisture, Teddington, 1998. |
| [6] | DAVIS R.S., « Formule pour la détermination de la masse volumique de l´air humide (1981/1991) », Rapport de la 4e session du CCM, BIPM, 1991. |
| [7] | "Mixing ratio", Wikipedia, accéder à la page Wikipedia |
| [8] | « Formule pour la détermination de la masse volumique de l´air humide (1981) », BIPM, 1981. |
| [9] | « Mesure de l'humidité de l'air - Psychromètres - Caractéristiques », Afnor, 1996. |
| [10] | PLATEL F., « La conversion EIPT68/EIT90 », MetGen, DM 9. |
| [11] | MOHR P.J. et TAYLOR B.N., "2005 CODATA recommended values of the fundamental physical constants", Rev. Mod. Phys., 2002, 77, 1-107. |
| [12] | WIESER M.E., "2006 Atomic weights of the elements", Pure Appl. Chem., 2005, 78, 2051-2066. |
| [13] | PLATEL F., « Calcul symbolique sur ordinateur - Projet PFS-Algebraic Calculator », MetGen, Dossier divers 2. |